
沉寂已久的CDE又开始了每逢周末发公告的习惯,周五(10月28日)发布了《拟纳入优先审评程序药品注册申请的公示》,共29个受理号获得优先审评的机会。周六(10月29日)发布了关于征求《成人用药数据外推在儿科人群药物临床试验及相关信息使用的技术指导意见的通知》,这将促进儿科用药的研发热情,至少儿科人体临床试验的研究成本相对降低了,利好早已超适应人群的改良型规格的注册申报。
沉寂已久的CDE又开始了每逢周末发公告的习惯,周五(10月28日)发布了《拟纳入优先审评程序药品注册申请的公示》,共29个受理号获得优先审评的机会。周六(10月29日)发布了关于征求《成人用药数据外推在儿科人群药物临床试验及相关信息使用的技术指导意见的通知》,这将促进儿科用药的研发热情,至少儿科人体临床试验的研究成本相对降低了,利好早已超适应人群的改良型规格的注册申报。
CDE10月28日所公布的名单如下表,其中CXSL1600011曾在9月14日的《拟纳入优先审评程序药品注册申请的公示》中优先审评理由为病毒性肝炎公示过一次,本次则以乙型肝炎治疗药物为由再做申请。实际上,CDE自2016年4月18日的《拟纳入优先审评程序HCV药物注册申请的公示》发布之后的拟纳入优先审评程序药品注册申请的确定公告一直从缺。

仅有3个产品申报生产,分别是丽珠的具有明显临床价值的创新药和重大专项的艾普拉唑钠及其注射剂,以及恒瑞的首仿品种注射用紫杉醇(白蛋白结合型),2个申报生产的制剂产品都是注射剂,比对CFDA近期所公布的新药获批的产品可发现CFDA最近较为偏爱批产注射剂。
余下26个品规主要是申报临床,其中11个受理号属于丙型肝炎直接抗病毒治疗药物,3个属于艾滋病治疗药物,2个受理号属于乙型肝炎治疗药物。咸达数据V3.2发现,共26个受理号由于适应症为治疗丙型肝炎病毒感染而进入CDE优先审评审批名单。
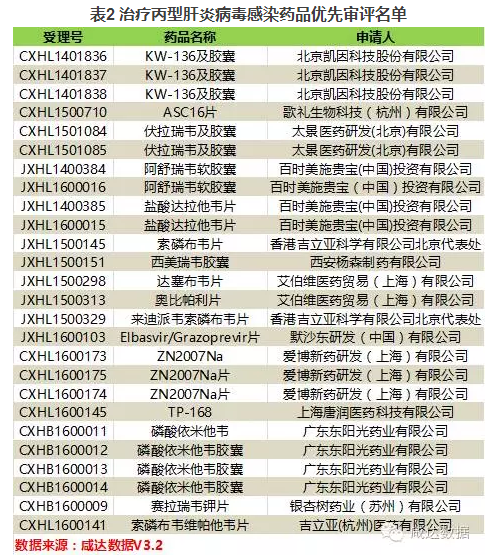
将2015年7月22日公告的自查核查名单作为“第一批自查”,2016年4月1日公告的作为“第二批自查”,9月1日公告的作为“第三批自查”,“第一批自查”共有11个受理号优先审评,“第二批自查”仅有4个受理号,“第三批自查”有6个受理号,包括丽珠的注射用艾普拉唑钠。以上21个受理号中,17个已经通知进行临床现场核查。预计一旦通过临床核查,这17个产品有望加速获批。
4个未通知临床现场核查但属于拟优先审评与自查目录的产品分别为爱可泰隆医药贸易(上海)有限公司的麦格司他胶囊、成都天台山制药有限公司麦格司他胶囊,四川鼎诺泰宸科技有限公司的左乙拉西坦注射液,贝达药业股份有限公司的氯法拉滨注射液和丽珠集团丽珠制药厂的注射用艾普拉唑钠。

 分享
分享
